CROの選び方
なぜCRO選びがプロジェクトの成否を分けるのか
非臨床・臨床試験におけるアウトソーシングの現状
近年の新薬開発は、バイオ医薬品や遺伝子治療、再生医療といったモダリティの多様化により高度に専門化しています。もはや自社のアセット(施設・人員)だけで全ての試験を完結させることは困難であり、特定の技術やノウハウを持つ外部専門組織への依存度はかつてないほど高まりました。現代のCROは単なる作業の「外注先」ではなく、科学的知見を共有し、共に開発を加速させる重要な「戦略的パートナー」へとその役割を変えています。
CRO選定ミスがもたらす3つのリスク(コスト増・納期遅延・品質低下)
不適切なCRO選定は、プロジェクトに致命的な打撃を与えます。
第一に、手技の未熟さによる試験のやり直しは数千万円単位のコスト増を招きます。
第二に、進捗管理の不備による納期遅延は、PMDA/FDAへの申請を遅らせ、1日あたり数億円とも言われる市場独占機会の損失に直結します。
第三に、データの信頼性不足という品質低下は、承認申請の却下や開発中断という最悪の結末を引き起こします。
「目先の安さ」のみで選ぶことは、極めてハイリスクな賭けと言わざるを得ません。
「失敗しないCRO」の選定基準5選
1. 専門性と実績
「がん領域に強い」「中枢神経系に実績がある」など、特定の疾患領域や試験種別への深い知見を確認しましょう。過去の受託件数だけでなく、論文発表や学会活動を通じた学術的裏付けも重要です。類似の試験プロトコルの実施経験が豊富であれば、予期せぬトラブルへの回避能力も高く、信頼に値するパートナーと言えます。
2. 施設・設備の充実度
最新の3D画像解析や高感度な質量分析計など、試験に必要な設備が揃っているかは必須の確認事項です。一方で、施設の築年数よりも、厳格な動物飼育管理や停電時のバックアップ体制、デジタルデータ管理への対応度(CSV対応等)を重視すべきです。機器のメンテナンスが徹底されている現場には、データの精度も自ずと宿ります。
3. 信頼性と品質保証
GLP基準の厳格な遵守はもちろん、独立した品質保証(QA)部門が適正に機能しているかを確認します。特に米国FDAや欧州EMAへの国際申請を視野に入れている場合は、海外当局による査察経験の有無が成否を分けます。過去の指摘事項に対する改善状況など、透明性の高い情報開示姿勢も選定の大きなポイントとなります。
4. コミュニケーションと柔軟性
担当者の科学的バックグラウンドや、トラブル時のレスポンスの速さは、試験の質に直結します。指示を待つだけの受身な姿勢ではなく、試験デザインの最適化に向けた専門的な提案があるかを見極めてください。委託側が「丸投げ」にせず、互いに科学的な議論を戦わせ、柔軟に調整できる関係性こそがプロジェクトを成功へ導きます。
5. 費用対効果
初期見積もりの低さだけで判断するのは危険です。追加費用の発生条件や、すばやく試験を成功させる確実性を含めた「トータルコスト」で比較してください。安価なCROに依頼してデータが使えず、他社で再試験を行う「セカンドオピニオン費用」は大きな損失です。最終的な投資対効果(ROI)を冷静に見極める眼力が必要です。
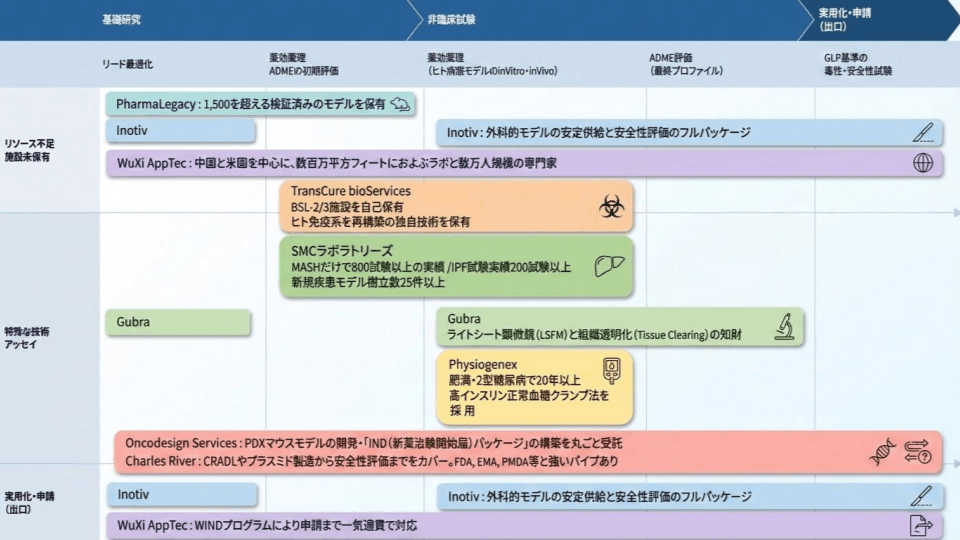
主要CROのポジショニングマップと特徴比較
創薬試験の開発フェーズは、基礎研究に始まり初期評価、ADMEとヒト病態モデルでの薬効薬理試験を経て、最終的にGLP基準の毒性・安全性試験を行い、FITへと移ります。創薬研究のフェーズや自社の課題によって選定すべきCROは変わります。
現在の創薬トレンド(代謝・がん)において外せない標準モデルを持つ企業や特定の高度技術で世界的に評価されている独立系企業を中心に9社ピックアップしました。
調査期間:2026年1~3月。
主要CROの特徴比較
国内大手・独立系・外資系の違いと使い分け
外資大手はグローバル同時申請に強みを持つ一方、コスト高で小回りが利きにくい傾向があります。対して国内大手はPMDA対応に厚い信頼があり、国内申請の要所を熟知しています。さらに独立系は特定のアッセイに特化し、迅速かつ柔軟な対応が可能です。プロジェクトの規模や目的に応じた最適な使い分けが求められます。
【特定領域に強い】ブティック型CROの活用メリット
特定の疾患モデル(例:NASH/MASHのSTAMマウス等)を独占的に保有するCROや、特殊技術を持つ小規模な「ブティック型」CROには独自の強みがあります。大手には真似できない「尖った技術」が必要な創薬初期フェーズにおいて、これらの専門機関は圧倒的な試験効率と精度の高いデータを提供します。ニッチな課題に対して、最短距離で解決策を導き出せるのが最大のメリットです。
CRO選定から委託開始までの具体的なステップ
Step 1:RFP(提案依頼書)の作成と要件定義
CRO選定の第一歩は、試験の目的、期間、予算、必要なデータ精度を明文化したRFP(提案依頼書)の作成です。この要件定義が曖昧だと、各社から提出される見積もりの前提条件がバラバラになり、適切な比較検討が不可能になります。自社が求める成果物のレベルを詳細に提示することが、精度の高い提案を引き出す鍵となります。
Step 2:秘密保持契約(NDA)の締結と候補の絞り込み
具体的な情報の開示に先立ち、迅速に秘密保持契約(NDA)を締結します。その後、RFPに基づき数社へ初期ヒアリングを実施しましょう。専門性や概算費用、納期対応の可否を確認し、自社の要件を満たさない会社をこの段階で適切に足切りすることで、次ステップの施設見学や詳細評価の効率を大幅に高めることができます。
Step 3:施設見学(オーディット)でチェックすべきポイント
施設見学では、現場の清潔感や機器の校正ラベル、生データの保管状況、スタッフの教育記録を厳格に確認します。特に重要なのは「現場の人間が誇りを持って働いているか」という非言語情報です。手順書(SOP)の遵守状況だけでなく、細部への配慮や誠実な姿勢があるかは、データの信頼性を左右する本質的な要素となります。
Step 4:見積もり比較と最終決定
最終段階では、各社の価格だけでなく提案内容(試験デザインや手法)の妥当性を総合的に判断します。単に安い方を選ぶのではなく、提示されたMethodが科学的に最適か、リスク対策は十分かを吟味してください。価格と質のバランスが自社のプロジェクト戦略に最も合致する1社を、根拠を持って選定することが重要です。
グローバル展開を見据えたCRO選びのポイント
海外拠点の有無とネットワークの強み
海外での現地試験が可能か、現地の提携網が強固かを確認します。特に、生体サンプルの国際輸送におけるロジスティクス体制や、通関トラブルへの対応実績は、グローバル試験のスケジュールを左右する重要事項です。
多言語対応と海外規制当局への知見
英語での質の高い報告書作成能力はもちろん、FDAやEMAからの照会事項(クエリ)に対する回答支援の実績を重視しましょう。海外当局の要求水準を熟知しているCROは、世界市場への進出を強力に後押しします。
まとめ:自社のニーズに最適なパートナーを見つけよう
CRO選びの成否は、新薬開発のスピードと品質を左右する極めて重要なプロセスです。自社のプロジェクト規模や疾患領域、将来的なグローバル展開の有無を整理し、今回ご紹介した5つの選定基準に照らし合わせて、最適なパートナーを見極めてください。